Доставка генов в клетку
Друзья, с момента основания проекта прошло уже 20 лет и мы рады сообщать вам, что сайт, наконец, переехали на новую платформу.
Какое-то время продолжим трудится на общее благо по адресу
На новой платформе мы уделили особое внимание удобству поиска материалов.
Особенно рекомендуем познакомиться с работой рубрикатора.
Спасибо, ждём вас на N-N-N.ru
Одним из наиболее перспективных вариантов систем доставки генов в клетки являются полиплексы – комплексы переносимой ДНК и катионных полимеров различной природы. В данной статье описываются свойства полиплексов на основе нескольких типов катионных полимеров, их транспорт в ядра клеток-мишеней, а также один из подходов для лечения злокачественных новообразований с помощью этих конструкций.
Введение
Генная терапия – лечение наследственных, онкологических и других заболеваний путём внесения в клетки пациента необходимого генетического материала с целью направленного изменения генных дефектов или придания клеткам новых функций [Горбунова и др., 1997]. Для доставки ДНК или РНК в клетки-мишени создаются носители (векторы) для обеспечения высокого уровня трансфекции, т.е. переноса экзогенной (чужеродной) ДНК или РНК в определённые типы клеток. Помимо этого, векторы должны обеспечивать защиту генетической информации, т.к. в условиях in vivo чужеродная ДНК нестабильна из-за быстрой деградации сывороточными нуклеазами [Dunlap et al., 1997], ферментами, расщепляющими нуклеиновые кислоты.
Типы транспортёров генетического материала
В природе существуют специализированные структуры для доставки генетической информации в клетки – вирусы. Поэтому их начали использовать в качестве транспортёров генов. В то же время использование вирусных векторов имеет целый ряд ограничений. Во-первых, это малая ёмкость переносимого генетического материала и свойственная вирусам собственная клеточная специфичность. Во-вторых, это возможность вирусов возвращения к дикому типу в результате рекомбинации при прохождении однотипной инфекции. В-третьих, белки вирусных частиц обладают высокой иммуногенностью, в результате чего повторное их введение вызывает иммунный ответ. Наконец, массовое производство вирусных векторов всё ещё достаточно проблематично и требует больших затрат. В настоящее время активно разрабатываются различные варианты невирусных носителей на основе катионных липидов и катионных полимеров. Эти катионные молекулы способны спонтанно формировать самособирающиеся нанокомплексы с отрицательно заряженной молекулой ДНК за счёт электростатических взаимодействий. Самособирающиеся комплексы, состоящие из катионных липидов и ДНК, называют липоплексами, состоящие из катионных полимеров и ДНК – полиплексами.
Катионные полимеры, используемые для создания полиплексов
Для целей генотерапии и биотехнологии предложено большое количество катионных полимеров или поликатионов. Поликатионы конденсируют ДНК в компактные нанокомплексы, обеспечивая стабильность ДНК и защиту от действия нуклеаз. В качестве ДНК-связывающих полимеров могут служить катионные белки, синтетические гомополимеры аминокислот (полилизины, полиаргинины), полисахарид хитозан, полиэтиленимин, дендримеры различного состава и другие модифицированные полимеры [Park et al., 2006]. Степень компактизации ДНК определяется суммарным зарядом комплекса, который, в свою очередь, зависит от отношения количества положительных групп полимеров к числу отрицательных фосфатных групп ДНК. Обычно в составе полиплексов поликатион находится в избытке, в результате чего формируются наноразмерные комплексы (от нескольких десятков до нескольких сотен нм), которые растворимы в воде и положительно заряжены (рис. 1, 2). В противном случае комплексы будут нестабильны.
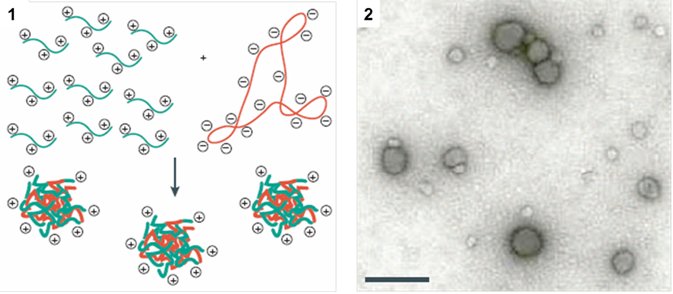 Рис. 1. Схема образования полиплексов из катионных полимеров и кольцевой молекулой ДНК (плазмидой) [Pack et al., 2005]. Рис. 2. Изображение полиплексов на подложке, полученное с помощью трансмиссионной электронной микроскопии (деление шкалы 200 нм), [Pack et al., 2005].
Рис. 1. Схема образования полиплексов из катионных полимеров и кольцевой молекулой ДНК (плазмидой) [Pack et al., 2005]. Рис. 2. Изображение полиплексов на подложке, полученное с помощью трансмиссионной электронной микроскопии (деление шкалы 200 нм), [Pack et al., 2005].
Одним из первых применяемых для доставки генов поликатионов был поли-L-лизин (ПЛ, рис. 3), который благодаря своей пептидной природе является биодеградабельным, что делает его крайне удобным для использования in vivo. Часто для устранения нежелательных эффектов, связанных с высокой плотностью поверхностного заряда, применяют сополимер ПЛ с полиэтиленгликолем (ПЭГ), [Pack et al., 2005]. В результате такой модификации уменьшается поверхностный заряд комплекса, что предотвращает неспецифическую адсорбцию отрицательно заряженных сывороточных белков крови на полиплексах, а также уменьшает цитотоксичность комплексов.
Полиэтиленимин (ПЭИ, рис. 3) считается одним из наиболее перспективных вариантов поликатионов для создания полиплексов на его основе. ПЭИ синтезируют в двух формах: линейной и разветвлённой. ПЭИ обладает большим количеством амино- и иминогрупп, способных к протонированию, в результате чего он проявляет буферные свойства при физиологических условиях. Полиплексы на основе ПЭИ отличаются более эффективной трансфекцией и защитой от действия нуклеаз по сравнению с другими поликатионами, что связано с высокой плотностью зарядов на ПЭИ и более компактным сворачиванием ДНК. Сильный положительный заряд приводит к токсичности ПЭИ, что вместе с отсутствием биологического разложения ПЭИ являются лимитирующими факторами для использования ПЭИ in vivo. С целью снижения цитотоксичности ПЭИ модификацируют с помощью полиэтиленгликоля, обладающего низкой токсичностью и высокой гидрофильностью.
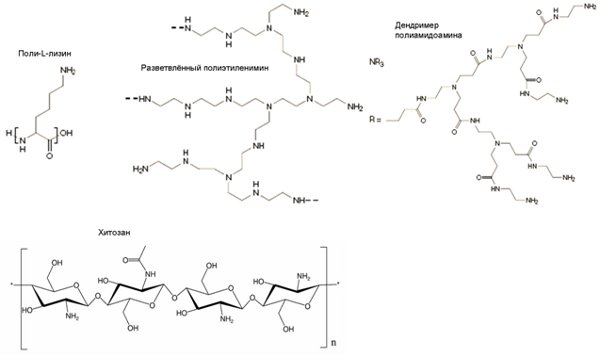 Рис. 3. Катионные полимеры, используемые для создания полиплексов, [Pack et al., 2005] и [Park et al., 2006].
Рис. 3. Катионные полимеры, используемые для создания полиплексов, [Pack et al., 2005] и [Park et al., 2006].
Другим представителем поликатионов, используемых в доставке генетической информации являются полиамидоамины (ПАМАМ, рис. 3). Эти соединения представляют собой сильноветвящиеся дендримеры. Благодаря ветвлению ПАМАМ обладают большой гибкостью, в лучшей степени компактизуют ДНК, полиплексы на их основе более стабильны, чем все остальные, [Pack et al, 2005]. По своим свойствам имеет много общего с ПЭИ.
Хитозаны (рис. 3) представляют собой полисахариды, построенные из D-глюкозамина и N-ацетил-D-глюкозамина, связанных (1>4) гликозидными связями. В зависимости от молекулярного веса и степени деацетилирования хитозаны формируют стабильные комплексы различной величины с переносимой ДНК. Маленькие, или наоборот, слишком большие полимеры хитозана ведут к снижению экспрессии переносимого гена. Основным достоинством полиплексов на основе хитозана является биодеградабельность, [Park et al., 2006].
На эффективность доставки полиплексов влияют многие факторы: молекулярный вес, степень разветвленности, полимеризации и тип полимера, размер частиц, ионная сила раствора, поверхностные заряды комплексов, а также условия проведения эксперимента. Оптимальный подход должен учитывать каждый из этих факторов и их влияние на свойства комплекса, поглощение клетками-мишенями комплексов, токсичность.
Существуют несколько подходов для обеспечения специфичности действия полиплексов на клетки-мишени. Один из них включает в себя адресную доставку нанокомплексов в определённые типы клеток. Этот подход связан с присоединением к полиплексам компонентов (лигандов), рецепторы к которым в большом количестве присутствуют на поверхности клеток-мишеней. В качестве специфичных лигандов используются различные белки, сахара, пептиды, антитела и т.д. Другая стратегия заключается в использовании таких транспортируемых генов, которые были бы активны только в определённых клетках, при этом доставка комплексов происходит неспецифично, то есть в любые клетки.
Проникновение полиплексов в клетки-мишени
Процесс доставки генетического материала включает два этапа: внеклеточный (путь от места введения до клеток-мишеней) и внутриклеточный (взаимодействие с клетками-мишенями, эндоцитоз, выход из эндосом, доставка в ядро). Внутриклеточные пути транспорта полиплексов представлены на рисунке 4.
Первым барьером, который необходимо преодолеть полиплексу на пути до клетки-мишени является кровь и внеклеточный матрикс. Именно поэтому необходимо подобрать такие физико-химические параметры комплекса, чтобы увеличить его стабильность, избежать неспецифических взаимодействий и возможности иммунного ответа. Во-первых, в составе полиплекса ДНК должна быть защищена от действия внеклеточных нуклеаз. Во-вторых, отрицательно заряженные белки сыворотки крови (альбумин, фибриноген, иммуноглобулины и др.), а также белки внеклеточного матрикса (коллагены) способны адсорбироваться на поверхности заряженных нанокомплексов, что ведет за собой изменение поверхностного заряда полиплексов, приводит к увеличению размера комплексов и к их агрегации. При введении полиплексов в организм они частично накапливаются в тканях и подвергаются фагоцитозу. По этим причинам часто применяют местное введение полиплексов (например, в опухоль при раке) в расчёте на их неспецифическое взаимодействие с клетками ткани.
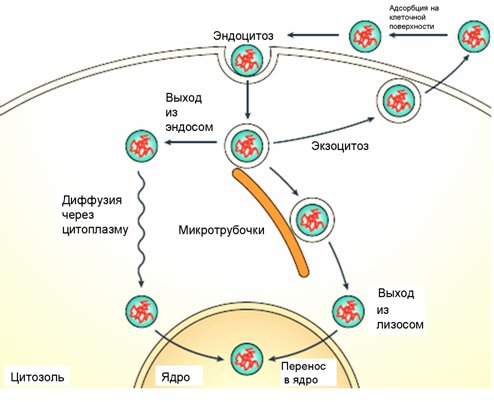 Рис. 4. Внутриклеточные пути транспорта полиплексов, [Pack et al, 2005].
Рис. 4. Внутриклеточные пути транспорта полиплексов, [Pack et al, 2005].
Полиплексы сначала адсорбируются на плазматической мембране, поглощаются путём эндоцитоза, после чего они должны покинуть эндолизосомы и пересечь ядерную оболочку для попадания в ядро. Существуют также альтернативные пути транспорта, не всегда приводящие к доставке комплексов в ядро. Помимо этого, для экспрессии переносимого гена необходима диссоциация полиплекса на катионный полимер и свободную ДНК.
Следующим этапом доставки генетического материала в клетки-мишени является их взаимодействие с плазматической мембраной и поглощение клеткой. Как было отмечено выше, связывание полиплексов с клетками в отсутствие лиганда происходит неспецифично в результате электростатического взаимодействия с отрицательно заряженной плазматической мембраной. В большинстве случаев такие полиплексы поглощаются путём неспецифического адсорбтивного эндоцитоза [Lechardeur et al., 2004]. При включении лиганда в состав комплекса можно добиться поглощения с помощью клатрин-зависимого рецептор-опосредованного эндоцитоза [De Smedt et al., 2004]. Другие пути захвата зависят от типа клеток и включают в себя фагоцитоз и кавеолин-зависимый эндоцитоз. Одна из стратегий для улучшения доставки полиплексов в клетку включает в себя использование вирусных проникающих пептидов, таких как TAT-пептид, впервые выделенный из вируса ВИЧ-1. Использование этих последовательностей обеспечивает попадание конструкций в клетку, и доставку полиплексов в клеточное ядро.
Одним из самых важных этапов транспортного пути полиплексов является их выход из эндосом. Как известно, эндосомы представляют собой систему трубочек и пузырьков, что необходимо для сортировки поглощённых макромолекул. Сортирующие эндосомы расположены ближе к плазматической мембране [Maxfield et al., 2004]. За счёт работы протонных помп в них понижается рН (около 6,5 в сортирующих эндосомах). Дальнейший транспорт может идти либо по пути рециркуляции с выбросом поглощённых молекул во внемембранное пространство, либо по литическому пути, когда происходит дальнейшее закисление среды в поздних эндосомах, и макромолекулы поступают в лизосомы. В лизосомах содержимое закисляется до рН 5, и поглощенные молекулы деградируют под действием гидролитических ферментов, которые активируются при низком рН. Продукты деградации удаляются из клетки путём экзоцитоза или переносятся в цитоплазму, где используются как строительный материал.
Считается, что полиплексы на основе ПЭИ в силу своих свойств способны выходить из эндосом благодаря так называемому эффекту «протонной губки» (proton sponge effect). Эта гипотеза [Pack et al., 2005] основана на том, что катионные полимеры за счёт наличия непротонированных вторичных и третичных аминов создают буферный эффект, в результате чего H±АТФаза, накачивающая протоны в эндосомы, начинает работать активнее. При этом происходит накопление внутри эндосом анионов хлора. В результате из-за резкого увеличения осмотического давления происходит набухание и лизис, что позволяет полиплексам попасть в цитозоль неповреждёнными. Предложен и другой механизм выхода из эндосом для полиплексов, который заключается в дестабилизации эндосомальной мембраны из-за высокой поверхностной плотности заряда нанокомплексов [Lechardeur et al., 2004]. Комплексы на основе ПЛ и хитозана не вызывают эффекта «протонной губки» и в меньшей степени способны дестабилизировать мембрану эндосом, что приводит к гораздо меньшей эффективности трансфекции.
Выйдя из лизосом, полиплексы оказываются в перинуклеарном пространстве, после чего комплекс диссоциирует на свободный поликатион и ДНК. Считается, что это происходит за счёт конкуренции за катионные группы между фосфатными группами ДНК и низкомолекулярными соединениями и анионами цитоплазмы. В некоторых случаях диссоциация комплекса происходит, по-видимому, в ядре. Главным барьером на пути плазмидной ДНК в клеточное ядро служит двойная ядерная оболочка. Для доставки в ядро макромолекул в их состав включают последовательность ядерной локализации (ПЯЛ), которая в комплексе с ?- и ?-импортинами будет узнаваема ядерным поровым комплексом (ЯПК) и активно проникать внутрь ядра. Через ЯПК путём пассивной диффузии могут проходить только маленькие молекулы (<40 кД, ~10 нм). Так как освободившаяся после распаковывания комплекса свободная плазмидная ДНК не имеет последовательности ядерной локализации, то в ядро будет проходить очень незначительная часть плазмид (не более 0,1–0,001%). Кроме того, установлено, что около 50% инъецированной ДНК деградирует в цитозоле уже через 1–2 часа после введения [Lechardeur et al., 2004]. Но т.к. клетки опухолей, против которых и направлена генная терапия, отличаются активной пролиферацией, то ДНК без труда проникает в ядра дочерних клеток во время митотического цикла, когда ядерная оболочка демонтирована.
Механизмы действия терапевтических генов
После проникновения плазмиды в ядро начинается экспрессия терапевтического гена. Для придания специфичности действия полиплексам терапевтический ген в составе плазмиды ставится под контроль промотора (область гена, на которую садится РНК-полимераза перед транскрипцией), активного только в опухолевых тканях. Примерами могут служить промотор гена антиапоптозного белка сурвивина или гена фермента теломеразы. В качестве терапевтического гена может быть использован ген тимидинкиназы вируса простого герпеса (HSVtk), которая обладает способностью фосфорилировать антигерпесные соединения ацикловир и ганцикловир [Reid et al., 1988]. Эти соединения вводятся в опухоль спустя некоторое время. Далее клеточные киназы (фосфорилирующие ферменты) превращают фосфорилированные ацикловир или ганцикловир в трифосфаты, которые способны включаться во вновь синтезированную ДНК во время удвоения при клеточном делении и терминировать её синтез. В результате клетки, в ядра которых попал ген тимидинкиназы, уничтожаются в присутствии этих веществ. При этом погибают именно делящиеся клетки, а не покоящиеся, которые не синтезируют ДНК и не включают ганцикловир или ацикловир. Такой механизм действия терапевтического гена можно использовать для целей генной терапии раковых опухолей, клетки которых быстро делятся.
Список литературы:
- Горбунова В.Н., Баранов В.С. Введение в молекулярную диагностику и генотерапию наследственных заболеваний. С.-Пб., «Специальная литература», 1997, с.287.
- Dunlap D.D., Maggi A., Soria M.R., Monaco L. Nanoscopic structure of DNA condensed for gene delivery. //Nucl. Acids. Res., 1997, vol. 25, 3095–3101.
- Park T.G., Jeong J.H., Kim S.W. Current status of polymeric gene delivery systems. // Adv. Drug Deliv. Rev., 2006, vol. 58, 467– 486.
- Pack D. W., Hoffman A. S., Pun S. and Stayton P. S. Design and development of polymers for gene delivery. // Nature Rev., Drug Discovery, 2005, vol. 4, 581.
- Lechardeur D., Verkman A.S., Lukacs G. L. Intracellular routing of plasmid DNA during non-viral gene transfer. // Adv. Drug Deliv. Rev., 2005, vol. 57, 755– 767.
- Maxfield F.R. and McGraw T.E. Endocytic Recycling. // Nature Rev. Mol. Cell. Biol., 2004, vol. 5, 121–132.
- Reid R., Eng-Chung M., Eng-Chang H. and Topal M.D. Insertion and extension of acyclic, dideoxy, and ara nucleotides by herpesviridae, human alpha and human beta polymerases. // J. Biol. Chem., 1988, vol. 263, 3898–3904.
Дурыманов Михаил, студент Биологического факультета МГУ
Статья – призер научно-популярного конкурса на конференции «Ломоносов 2009» (Биологический факультет, секции «Нанобиотехнология», «Биоинженерия», «Биофизика».
- Источник(и):
- Войдите на сайт для отправки комментариев
 Сайт о нанотехнологиях #1 в России
Сайт о нанотехнологиях #1 в России