Малые молекулы для «GPS-навигации» стволовых клеток
Биоинженеры из Женской больницы Бригема (Brigham and Women's Hospital, BWH) и сотрудники фармацевтической компании Sanofi нашли малые молекулы, которые могут быть использованы для «сопровождения» стволовых клеток к месту повреждения, заболевания или воспаления. Кроме того, предлагая новую стратегию адресной доставки клеток, важными инструментами в дальнейшем развитии клеточной терапии могут стать и сами методы, использованные для поиска и тестирования этих низкомолекулярных соединений. Результаты работы опубликованы в онлайн издании журнала Cell Reports.
Исследователи протестировали более 9000 соединений, и, используя многоступенчатый подход – в том числе сложные микрофлюидные устройства и новые технологии визуализации, – сузили область поиска, чтобы проверить наиболее перспективные из найденных.
«В нашем распоряжении множество методик и инструментов, которые могут быть использованы, чтобы манипулировать клетками вне организма и заставить их делать почти все, что нужно, но как только мы пересаживаем клетки, мы теряем полный контроль над ними», – говорит соавтор исследования Джефф Карп (Jeff Karp), PhD, адъюнкт-профессор BWH, Гарвардской медицинской школы (Harvard Medical School), главный преподаватель в Гарвардском институте стволовых клеток (Harvard Stem Cell Institute). «Благодаря этому сотрудничеству мы смогли найти малые молекулы, которые могут быть использованы для обработки клеток вне организма и их программирования на таргетинг кровеносных сосудов в пораженных или поврежденных тканях».
Малые молекулы дают ученым несколько преимуществ, включая возможность использовать одну из безопасных и сравнительно простых процедур для предварительной обработки клеток перед их внутривенным введением.
«Мы остро нуждаемся в стратегиях, которые повысили бы клиническое значение клеточной терапии», – говорит соавтор исследования Орен Леви (Oren Levy), PhD, преподаватель медицине в BWH. «Что нужно для реализации надежд, связанных с клеточной терапией, это именно разработка безопасной, экономичной и простой в применении инженерной стратегии».
Ранее доктор Карп и его коллеги из BWH установили, что для химического связывания молекул – «GPS-навигаторов», направляющих эту клетку в зону воспаления – с поверхностью клетки можно использовать биоинженерные методы. Полученные ими данные подтверждали возможность адресной доставки клеток.
«В BWH мы заложили основы. Наши коллеги из Sanofi имеют большой опыт в скрининге малых молекул, глубоко понимают биологию и знают о неудовлетворенных потребностях. Кроме того, у них есть замечательная возможность переводить новые лекарственные препараты в клинику», – рассказывает доктор Карп.
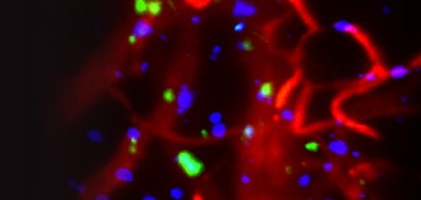 Ученые нашли низкомолекулярное соединение, с помощью которого можно осуществлять
Ученые нашли низкомолекулярное соединение, с помощью которого можно осуществлять
адресную доставку мезенхимальных стволовых клеток (синие и зеленые) в зону повреждения
или воспаления ткани. (Фото: Oren Levy, Brigham and Women's Hospital).
В поиске соединений, активирующих контрольные молекулы на поверхности мезенхимальных стволовых клеток (МСК), группа из Sanofi провела скрининг тысяч соединений, подтвердив при этом, что найденные ими активные вещества не изменяет жизнеспособность мезенхимальных стромальных клеток или профиль секретируемых иммуномодуляторных белковых факторов.
В настоящее время продолжаются или уже закончены клинические испытания более 450 методик использования МСК для лечения целого ряда заболеваний, включая инфаркт миокарда, болезнь Крона, волчанка, рассеянный склероз и др., но многие из тестируемых методик так и не становятся клиническими методами лечения. Одной из ключевых проблем здесь была и остается адресная доставка МСК (и длительное их там пребывание) к местам повреждения.
Исследователи выявили шесть самых мощных и перспективных молекул, в том числе соединение, известное как RO-31–8425. Затем, обработав ими клетки, лаборатория доктора Карпа протестировала эти соединения с помощью микрофлюидного устройства – предметного стекла с крошечными каналами, размер которых достаточен для того, чтобы одномоментно по ним могла проходить лишь небольшая группа клеток. Каналы микрофлюидного устройства были покрыты так называемыми внутриклеточными молекулами адгезии (Intracellular Adhesion Molecule, ICAM-1), присутствующими на поверхности кровеносных сосудов в воспаленной ткани. Предварительно обработанные Ro-31–8425 клетки застряли – показатель их способности к «самонаведению» на зоны воспаления.
Исследователи проверили свои результаты и на животных моделях. Они системно вводили предварительно обработанные Ro-31–8425 клетки мышам с одним воспаленным ухом. С помощью оптических методов визуализации (в частности, прижизненной микроскопии) они убедились в том, что обработанные этим соединением клетки не только накапливались и сохранялись в воспаленном ухе, но и уменьшали воспаление.
«Уникальную возможность достичь этого результата нам дало сотрудничество с нашими партнерами как из индустрии, так и из академической науки», – резюмирует доктор Крап. «Вместе мы решаем одну из основных проблем, стоящих перед клеточной терапией, – проблему адресной доставки стволовых клеток».
Оригинальная статья:
A Small-Molecule Screen for Enhanced Homing of Systemically Infused Cells
- Источник(и):
- Войдите на сайт для отправки комментариев
 Сайт о нанотехнологиях #1 в России
Сайт о нанотехнологиях #1 в России