Разработан вирусный вектор, селективно накапливающийся в кровеносных сосудах раковых опухолей
Ученые из Медицинской школы Вашингтонского университета (Washington University School of Medicine) в Сент-Луисе разработали метод доставки генов, крайне востребованный в генной терапии. Они создали дезактивированный вирус, который при введении в кровь доставляет тот или иной нужный ген в нужные клетки. В своих предварительных экспериментах на мышах исследователи подтвердили принципиальную возможность таргетинга кровеносных сосудов опухоли без негативного воздействия на здоровые ткани.
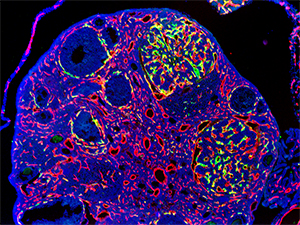 В одном случае первичная опухоль почки
В одном случае первичная опухоль почки
распространилась на яичник. Вирусные векторы,
собравшиеся в сосудах метастатической опухоли,
светятся зеленым. Красное окрашивание показывает
нормальные кровеносные сосуды яичника.
(Фото: JM Arbeit, DT Curiel)
«Большинство современных методов генной терапии, применяемых для лечения человека, связано с забором клеток из организма, их модификацией и возвращением обратно в организм пациента», – говорит Дэвид Кьюриел (David Curiel) MD, заслуженный профессор радиационной онкологии. «Это ограничивает применение генной терапии тканями, которые можно взять, обработать и вернуть пациенту, в частности, кровью и костным мозгом. Сегодня, через 30 лет исследований, мы все еще не можем ввести несущий ген вирусный вектор в кровоток и доставить ген в нужное место».
Профессору Кьюриелу и его коллегам из Онкологического центра Сайтмена (Siteman Cancer Center) при Школе медицины Вашингтонского университета и Барнес-Еврейской больнице (Barnes-Jewish Hospital) удалось разработать «самонаводящийся инъецируемый вектор» – дезактивированный вирус, мишенью которого является внутренняя оболочка кровеносных сосудов опухоли, не «застревающий» в печени – проблема, сводившая на нет предыдущие усилия ученых.
Статья о разработке опубликована в журнале со свободным доступом PLOS ONE.
Основываясь на своей предыдущей работе и разработках других ученых, исследователи сконструировали этот вирусный вектор таким образом, что доставляемые им гены включаются только в аномальных кровеносных сосудах, обеспечивающих опухоль питанием и энергией. Но в отличие от большинства методов лечения, направленных на опухолевые сосуды, ученые не ставили своей целью лишить опухоль кровоснабжения.
«Мы не хотим уничтожать опухолевые сосуды», – говорит руководитель исследования Джеффри Арбайт (Jeffrey Arbeit), MD, профессор урологической хирургии и клеточной биологии и физиологии. «Мы хотим захватить их и превратить в фабрики по производству молекул, которые изменяют микросреду опухоли так, что она больше не питает опухоль. Это может остановить рост опухоли как таковой или повысить эффективность стандартной химиотерапии и облучения. Одним из преимуществ новой стратегии является то, что она может быть применена почти ко всем самым распространенным раковым заболеваниям».
Теоретически, отмечает профессор Арбайт, такой подход может быть применен не только к раковым, но и к другим заболеваниям, для которых характерно поражение кровеносных сосудов, в том числе к болезни Альцгеймера, рассеянному склерозу и сердечной недостаточности.
Разработанный американскими учеными вирусный вектор содержит фрагмент ДНК под названием Robo4, активный в клетках, выстилающих кровеносные сосуды опухоли.
В экспериментах на мышах исследователи показали, что при введении в кровоток этот вирусный вектор в значительно большей степени накапливается в сосудистой сети опухоли, чем в легких, почках, сердце и других здоровых органах.
Чтобы убедиться в том, что вирусные векторы накапливаются в опухолях, избегая здоровых участков, исследователи использовали их для доставки гена, который просто заставлял выстилающие кровеносные сосуды клетки светиться зеленым.
Эксперименты проводились на мышах с опухолями в почках и клетками рака почек в коже. В одном случае опухоль в почке животного спонтанно метастазировала в яичник. Исследование показало, что кровеносные сосуды, питающие метастатические опухоли, светятся зеленым, чего не наблюдалось в сосудах здоровой части яичника.
Кроме того, добавление противосвертывающего препарата варфарина предупреждало накопление векторов в печени за счет блокирования взаимодействия вирусов с компонентами системы свертывания крови. Хотя исследователи подчеркивают, что лечение онкологических больных варфарином невозможно из-за риска развития кровотечений, предыдущая работа их группы показала возможность генетического манипулирования вирусным вектором для предотвращения его накопления в печени.
«Мы использовали комбинацию стратегий таргетинга», – комментирует профессор Кьюриел. «Мы объединили метод, разработанный нами для детаргетинга печени, и метод, мишенью которого являются кровеносные сосуды. Это сочетание позволило нам вводить вектор в кровоток мыши, и он обходил печень, находя интересующие нас пролиферирующие сосуды».
Оригинальная статья:
- Источник(и):
- Войдите на сайт для отправки комментариев
 Сайт о нанотехнологиях #1 в России
Сайт о нанотехнологиях #1 в России