Трехмодальные наночастицы позволяют удалять опухоли головного мозга с беспрецедентной точностью
Наночастицы, разработанные учеными Школы медицины Стэнфордского университета (Stanford University School of Medicine), позволяющие визуализировать опухолевую ткань одновременно тремя различными методами, сделали возможным удаление опухолей головного мозга у мышей с беспрецедентной точностью.
В статье, опубликованной он-лайн в журнале Nature Medicine, ученые во главе с профессором и заведующим кафедрой радиологии Сэмом Гамбхиром (Sam Gambhir), MD, PhD, показали, что разработанные ими адресные наночастицы позволяют определять локализацию опухолей головного мозга, точно очерчивая их границы и значительно облегчая их полное удаление. Этот новый метод может однажды помочь улучшить прогноз у пациентов со смертельным раком мозга.
Ежегодно только в США диагностируется около 14000 случаев раковых опухолей мозга, около 3000 из которых – глиобластомы, наиболее агрессивная форма рака головного мозга. Сегодня прогноз для пациентов с глиобластомой неутешителен: средняя продолжительность жизни без лечения составляет три месяца, а хирургическое удаление таких опухолей увеличивает выживаемость пациентов в среднем менее чем на год. Одна из главных причин неэффективности лечения заключается в том, что даже для самого опытного нейрохирурга практически невозможно полностью удалить опухоль, сохранив здоровую ткань мозга.
«При опухолях головного мозга хирурги не могут позволить себе роскошь удаления большого количества окружающих здоровых тканей мозга, чтобы гарантировать, что раковых клеток не осталось», – объясняет профессор Гамбхир. «Необходимо оставить неповрежденной как можно большую часть здоровой ткани».
Это серьезная проблема для глиобластомы, для которой особенно характерны нечеткие контуры. Крошечные пальцевидные выросты глиобластомы обычно проникают в здоровые ткани, распространяясь вдоль кровеносных сосудов и нервных путей. Еще одна опасность исходит от микрометастазов – мельчайших опухолей, образующихся в результате миграции и репликации клеток первичного новообразования. Усеивающие близлежащие здоровые ткани микрометастазы, невидимые для невооруженного глаза хирурга, могут развиться в новые опухоли.
Однако инновационные методы молекулярной визуализации могут изменить ситуацию в онкологической нейрохирургии, и исследование стэнфордских ученых демонстрирует возможность точного обнаружения опухолевой ткани до и во время операции с помощью высокотехнологичных наночастиц.
Разработанные ими наночастицы по существу представляют собой мельчайшие шарики из золота, покрытые визуализирующими химическими веществами. Их диаметр составляет около одной шестидесятой диаметра человеческого эритроцита.
«Мы предположили, что такие частицы, введенные внутривенно, будут преимущественно накапливаться в опухолях, а не в здоровых тканях мозга», – продолжает профессор Гамбхир, являющийся также научным сотрудником Стэнфордского онкологического института (Stanford Cancer Institute). «Крошечные кровеносные сосуды, питающие опухоль головного мозга, проницаемы, и поэтому мы надеялись, что эти сферы будут вытекать из сосудов и застревать в близлежащем опухолевом материале».
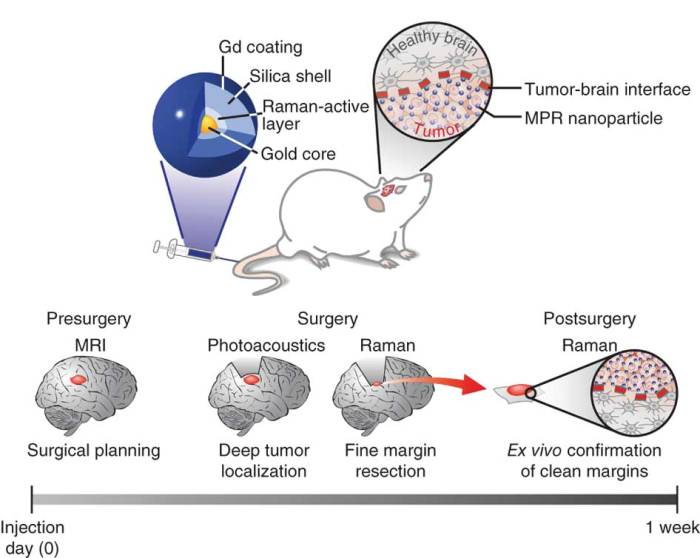 MPR-наночастицы вводятся внутривенно мышам с опухолями головного мозга (вверху). Циркулируя с кровотоком, наночастицы просачиваются через нарушенный гематоэнцефалический барьер, а затем поглощаются и сохраняются в опухолевой ткани. MPR-частицы слишком велики, чтобы преодолеть интактный гематоэнцефалический барьер и, следовательно, не могут накапливаться в здоровом мозге. Концепция предлагаемого клинического применения (внизу). Обнаруживаемость MPR-наночастиц с помощью МРТ позволяет определить локализацию опухоли в предоперационный период и спланировать ее хирургическое удаление. Так как частицы сохраняются в опухоли, достаточно одной инъекции, чтобы «видеть» их во время операции через несколько дней после введения. Фотоакустическая визуализация с ее относительно высоким разрешением и глубоким проникновением в ткани может обозначить объем резекции опухоли во время операции. Визуализация на основе комбинационного рассеяния с ее сверхвысокой чувствительностью и пространственным разрешением может быть использована для удаления микроскопических остатков опухоли. Впоследствии удаленной образец может быть изучен с помощью комбинационного рассеяния ex vivo для подтверждения поля опухоли. (nature.com/nm)
MPR-наночастицы вводятся внутривенно мышам с опухолями головного мозга (вверху). Циркулируя с кровотоком, наночастицы просачиваются через нарушенный гематоэнцефалический барьер, а затем поглощаются и сохраняются в опухолевой ткани. MPR-частицы слишком велики, чтобы преодолеть интактный гематоэнцефалический барьер и, следовательно, не могут накапливаться в здоровом мозге. Концепция предлагаемого клинического применения (внизу). Обнаруживаемость MPR-наночастиц с помощью МРТ позволяет определить локализацию опухоли в предоперационный период и спланировать ее хирургическое удаление. Так как частицы сохраняются в опухоли, достаточно одной инъекции, чтобы «видеть» их во время операции через несколько дней после введения. Фотоакустическая визуализация с ее относительно высоким разрешением и глубоким проникновением в ткани может обозначить объем резекции опухоли во время операции. Визуализация на основе комбинационного рассеяния с ее сверхвысокой чувствительностью и пространственным разрешением может быть использована для удаления микроскопических остатков опухоли. Впоследствии удаленной образец может быть изучен с помощью комбинационного рассеяния ex vivo для подтверждения поля опухоли. (nature.com/nm)
Золотые ядра частиц, имеющие покрытие из нескольких специализированных слоев, делают частицы видимыми одновременно для трех различных методов визуализации, каждый из которых вносит свой уникальный вклад в повышение эффективности хирургической операции.
Один из таких методов, магнитно-резонансная томография, уже часто используются, чтобы еще до операции указать хирургам, где находится опухоль. МРТ позволяет предварительно определить границы новообразования, но на момент самой операции этот метод не может идеально точно описать локализацию агрессивно растущей опухоли.
Наночастицы, разработанные группой Гамбхира, покрыты гадолинием – используемым в МРТ контрастным агентом. Покрытие разработано таким образом, что позволяет ему прочно связываться с относительно инертными сферами в крови и близких к ней средах. (В работе, опубликованной в 2011 году в журнале Science Translational Medicine, Гамбхир и его коллеги показали на животных моделях, что наночастицы, аналогичные используемым в новом исследовании, но не содержащие гадолиния, нетоксичны.)
Второй, более новый метод – фотоакустическая визуализация, при которой световые импульсы поглощаются материалами, такими как золотые ядра наночастиц. Частицы слегка нагреваются, генерируя ультразвуковые сигналы, которые могут быть обнаружены. Соответствующая обработка этой информации позволяет получить трехмерное изображение опухоли. Поскольку этот способ визуализации имеет большую глубину проникновения и очень чувствителен к присутствию частиц золота, он может быть полезен при удалении основной массы опухоли во время операции.
В третьем методе – визуализации на основе комбинационного рассеяния (рамановской визуализации) – используется способность определенных материалов (входящих в состав покрытия золотых сфер) генерировать практически не обнаруживаемые количества света с несколькими волнами различной длины. Поверхности золотых ядер усиливают слабые рамановские сигналы, и их можно уловить с помощью специального микроскопа.
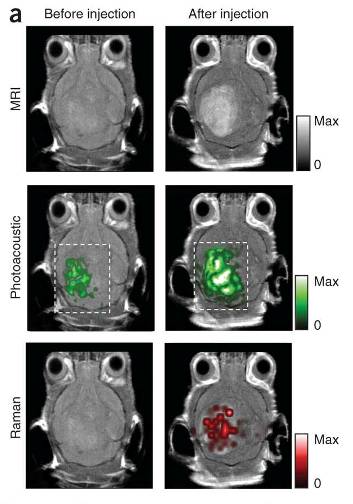 Двумерные МРТ, ФА и КР-изображения до (слева)
Двумерные МРТ, ФА и КР-изображения до (слева)
и после инъекции MPR-наночастиц.
(nature.com/nm)
Чтобы продемонстрировать преимущества своего подхода, ученые сначала показали, что специфической мишенью их наночастиц является опухолевая ткань и только опухолевая ткань. Затем они имплантировали несколько различных типов клеток человеческой глиобластомы глубоко в мозг лабораторных мышей. После введения наночастиц в вены хвоста мышей ученым удалось визуализировать, всеми тремя методами, развившиеся из клеток глиобластомы опухоли.
МРТ дала хорошие предоперационные изображения общей формы и расположения опухолей. А во время самой операции фотоакустическая визуализация обеспечила точную картину их границ в реальном времени, повысив эффективность хирургии.
Но ни МРТ, ни ФА-визуализация сами по себе не могут различить здоровые и раковые ткани на минимально достаточном уровне для обнаружения каждой оставшейся частицы опухоли. Здесь слово за третьим методом – визуализацией на основе комбинационного рассеивания. Рамановские сигналы исходят только от находящихся в опухоли наночастиц, но не от здоровых тканей, не содержащих источников сигналов. Таким образом, после того, как была удалена основная часть опухоли, очень чувствительный метод рамановской визуализации точно отображает остаточные микрометастазы и крошечные пальцевидные выросты опухоли, до сих пор скрывавшиеся в близлежащих здоровых тканях. Это, в свою очередь, позволяет удалить все опасные остатки.
«Теперь, еще до операции, мы можем узнать степень распространения опухоли и ориентироваться с молекулярной точностью во время самой процедуры удаления. Сразу же после этого мы можем «видеть» ранее невидимую остаточную опухолевую ткань и удалить и ее», – заключает профессор Гамбхир.
Кроме того, способность наночастиц нагреваться при ФА-стимуляции в сочетании с их специфичностью по отношению к опухолевой ткани может позволить применять их не только для визуализации, но и для селективного уничтожения опухолей, а достигаемая в этом случае хирургическая точность может быть использована при удалении и других типов опухолей.
Аннотация к статье:
- Источник(и):
- Войдите на сайт для отправки комментариев
 Сайт о нанотехнологиях #1 в России
Сайт о нанотехнологиях #1 в России