Новые формы поваренной соли нарушают правила химии
Открытие того, что при повышенном давлении могут существовать такие стабильные формы хлорида натрия, как NaCl3l и Nal3lCl, демонстрируют, что следует пересмотреть некоторые основные законы химии. Именно так утверждает Артем Оганов (Artem Oganov) из Университета Нью-Йорка, исследовательская группа которого предсказала, а затем и экспериментально доказали возможность существования этих необычных форм.
Как отмечает Оганов, такие
фундаментальные правила, как, например, правило баланса зарядов и правило устойчивых октетных оболочек могут быть нарушены при уже относительно скромных давлениях. Он добавляет, что даже для хорошо изученной системы можно подобрать условия, при которых будут появляться состояния с необычным строением и свойствами, заслуживающими дальнейшего изучения.
Исследователи из группы Оганова разработали компьютерный алгоритм, основанный на ab initio принципах квантовой механики, получивший название USPEX и позволяющий предсказывать кристаллические структуры, которые будет образовывать вещество определенного состава при определенном давлении и температуре.
С помощью этого алгоритма исследователи моделируют структуры, нарушающие базовые химические принципы и смотрят, насколько эти структуры энергетически выгодны или, наоборот, невыгодны.
Оганов поясняет, что
при изменении ряда внешних условий, таких как давление и температура, энергетическое состояние различных структур могут меняться, и запрещенные при нормальных условиях стабилизируются.
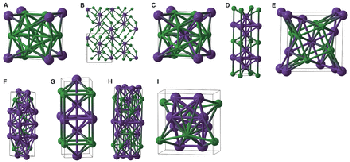 Рис. 1. При повышенном давлении обычная
Рис. 1. При повышенном давлении обычная
поваренная соль может образовывать экзотические
структуры, в которых соотношение ионов натрия
и хлора отличается от привычного соотношения 1:1.
Для алгоритма USPEX обычный хлорид натрия с соотношением ионов 1:1, которое подчиняется и зарядовому балансу и правилам устойчивых валентных оболочек, оказалась простой задачей. После первоначальных расчетов, показавших возможность существования при определенных условиях запрещенных структур, Оганов обратился к Вейвею Жаню (Weiwei Zhang), с просьбой экспериментально проверить правильность результатов моделирования.
В ходе экспериментов Жаню удалось доказать, что
при давлении, достигающем 250 ГПа, могут быть получены предсказанные теоретически Na3Cl, Na2Cl, Na3Cl2, NaCl3 и NaCl7, при этом у этих форм хлорида натрия наблюдается интересный тип связывания и электронные свойства. Однако при этом давлении классический NaCl еще сохраняет устойчивость и не распадается на другие соединения. Было выяснено, что для образования экзотических форм хлорида натрия требуется высокая температура и избыток либо натрия, либо хлора.
Дальнейшие эксперименты Оганова с соавторами заключались в том, что они подвергали поваренную соль экстремальному давлению на алмазной наковальне, поддерживая давление от 10 до 80 ГПа. Исследование образующихся фаз с помощью рентгеновской дифракции и спектроскопии комбинационного рассеивания показали, что при повышенном давлении в условиях нагревания и при избытке хлора образуется две фазы NaCl3, одна при давлении выше 18 ГПа, а другая – при давлении выше 54 ГПа.
Нагревание в присутствии избытка натрия приводит к тому, что при давлении выше 20 ГПа образуется Na3Cl.
Яньмин Ма (Yanming Ma) из Университета Цилинь (Китай), также изучающий структуры NaCl при повышенном давлении, говорит, что новые структуры весьма интересны. Он подчеркивает, что
высокое давление может служить ценным инструментом для синтеза новых материалов, нарушающих как известные закономерности, так и закономерности химии высоких давлений.
- Источник(и):
-
1. chemport.ru
- Войдите на сайт для отправки комментариев
 Сайт о нанотехнологиях #1 в России
Сайт о нанотехнологиях #1 в России
Очень любопытное исследование. Практическая польза, пока, не просматривается, но полученные соединения очень интересны.