Описаны механизмы увеличения энергии электронов в химических реакциях
Ученые описали, как можно увеличить энергию электронов в ходе химических реакций. Принципы этого процесса используются в химическом синтезе, однако детально их ранее не исследовали. Работа выполнена при поддержке гранта РНФ и опубликована в журнале Angewandte Chemie.
Движущая сила любого процесса в химии — это энергия. Направление ее потоков, контроль над ними, сохранение и расходование определяется всего тремя видами частиц: фотонами, электронами и протонами.
«Известны соединения, одна молекула которых способна принять два низкоэнергетических «холодных» фотона и «превратить» их в один высокоэнергетический «горячий», — рассказывает соавтор работы Михаил Сыроешкин, старший научный сотрудник Института органической химии имени Н.Д. Зелинского РАН. — Либо две молекулы могут принять по «холодному» фотону и вместе вернуть один «горячий» (естественно, с определенными комиссионными энергетическими сборами). Это явление называется ап-конверсией фотона, и оно известно уже более полувека. Подобное повышение энергии возможно и для других распространенных средств обмена, электронов, но для них подобные вопросы ранее не рассматривались».
Существует группа химических процессов, называемых экзергоническими, в результате которых система реагентов выделяет энергию. Авторы показали, как использовать эту энергию для того, чтобы находящийся в молекуле электрон приобретал дополнительную энергию. Принципы ап-конверсии задействованы во многих природных механизмах — от свечения светлячков до восстановления поврежденной ДНК. Также на них основано действие ферментов — природных катализаторов, которые ускоряют химические реакции.
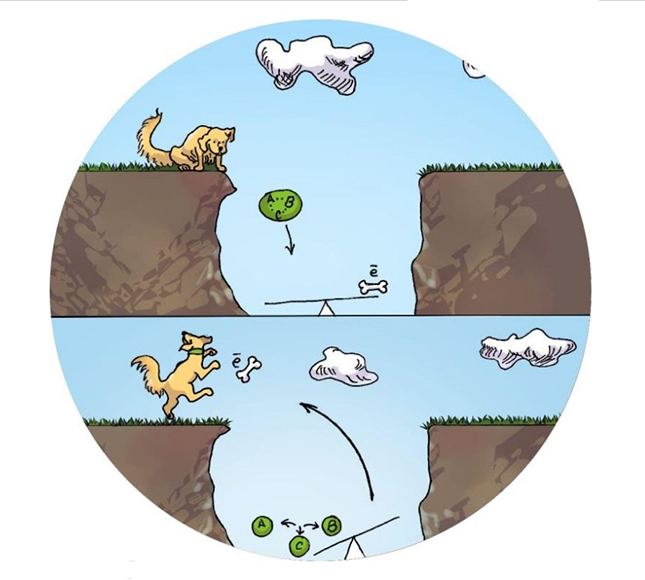 Принцип ап-конверсии: «поднять» энергию электрона, «уронив» энергию субстрата с разрушением в нем химических связей. Владислава Тимофеева
Принцип ап-конверсии: «поднять» энергию электрона, «уронив» энергию субстрата с разрушением в нем химических связей. Владислава Тимофеева
В новой работе ученые рассмотрели, как именно экзергонические реакции могут стимулировать ап-конверсию электронов. В живой системе низкоэнергетический электрон доступен, и если его перенести на химически активное соединение, то ап-конверсия может запустить «реакционный взрыв». Это полезно для реакций, которые катализируются при переходе электрона, в том числе в интенсивно развивающейся области фоторедокс-катализа, которая позволяет синтезировать, например, циклические соединения. Здесь ап-конверсия электрона — ключевой участник цикла: электрон играет роль челнока в цепочке химических реакций, путешествуя от молекулы к молекуле, переходя из состояния с низкой энергией в состояние с большой и обратно. В результате с использованием одного электрона можно получить большее количество продукта.
«Между тем, возможность протекания ап-конверсии электрона в том или ином случае может быть надежно выявлена с помощью современных квантовохимических и экспериментальных методов, — заключает ученый. — Следовательно, данное явление послужит основой для новых каталитических процессов и будет иметь не только концептуальное значение, но и предсказательную силу».
- Источник(и):
- Войдите на сайт для отправки комментариев
 Сайт о нанотехнологиях #1 в России
Сайт о нанотехнологиях #1 в России