Из стволовых клеток получены два типа строительных блоков для новых кровеносных сосудов
Вырастить в лаборатории новый кровеносный сосуд – сложнейшая задача, но группе инженеров из Университета Джонса Хопкинса (Johns Hopkins University) удалось разрешить основную проблему – как добиться, чтобы стволовые клетки образовывали два различных типа тканей, оба из которых в равной степени необходимы для построения мельчайших венозных и артериальных сетей.
 Шэрон Герехт (Sharon Gerecht), PhD,
Шэрон Герехт (Sharon Gerecht), PhD,
доцент кафедры химической и
биомолекулярной инженерии
Университета Джонса Хопкинса.
(Фото: Will Kirk/Homewood Photography)
Как исследователи достигли такого успеха, подробно изложено в статье, опубликованной в журнале Cardiovascular Research. Значение этой работы трудно переоценить, так как трансплантация выращенной в лаборатории сети новых сосудов может принести пользу огромному количеству пациентов, чья кровеносная системы поражена сердечно-сосудистыми заболеваниями, диабетом и другими болезнями.
«Наша долгосрочная цель – дать врачам новый инструмент для лечения пациентов с заболеваниями сосудов, несущих кровь ко всем органам» – говорит руководитель исследования Шэрон Герехт (Sharon Gerecht), PhD, доцент кафедры химической и биомолекулярной инженерии.
Группа доктора Герехт сфокусировала свое внимание на гладкомышечных клетках, находящихся в стенках кровеносных сосудов. Известно 2 типа таких клеток: синтетические гладкомышечные клетки, мигрирующие в пределах окружающей ткани, продолжающие делиться и поддерживающие вновь образующиеся кровеносные сосуды; сократительные клетки гладкой мускулатуры сосудов, остающиеся на месте, стабилизирующие рост новых сосудов и помогающие им поддерживать нужное давление крови.
В своих экспериментах по получению гладкомышечных клеток доктор Герехт и ее коллеги проводили эксперименты как на эмбриональных, так и на индуцированных плюрипотентных стволовых клетках – зрелых дифференцированных клетках, генетически перепрограммированных в клетки, близкие по свойствам к эмбриональным стволовым.
В одном из более ранних исследований им уже удалось индуцировать дифференциацию стволовых клеток в ткань, которая была близка к гладкомышечной, но все же отличалась от нее функционально. В своей новой работе исследователи экспериментировали с концентрациями добавляемых к стволовым клеткам ростовых факторов и сыворотки. Большие количества сыворотки и факторов роста «заставляли» стволовые клетки превращались в синтетические клетки гладкой мускулатуры, а при добавлении гораздо меньшего количества этих веществ они становились сократительными клетками.
По мнению доктора Герехт, возможность контролировать тип получаемых в лаборатории гладкомышечных клеток может иметь решающее значение для выращивания новых сосудистых сетей.
«Когда мы строим магистральный сосуд, поставляющий кровь, нужны сократительные клетки, обеспечивающие их структуру и стабильность, но в работе с очень мелкими кровеносными сосудами более полезными могут быть мигрирующие синтетические клетки», – объясняет ученый.
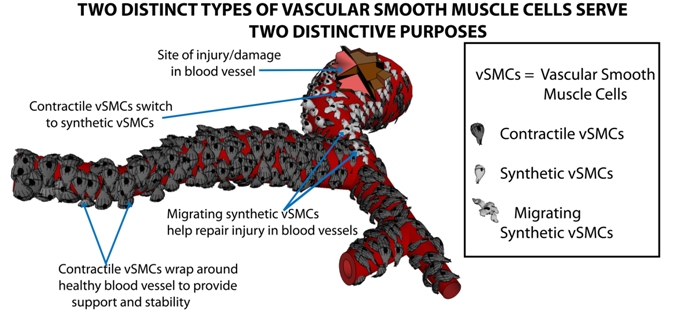 Два типа клеток гладкой мускулатуры сосудов выполняют разные функции. Сократительные клетки (contractile vSMCs) покрывают поверхность здорового сосуда,
Два типа клеток гладкой мускулатуры сосудов выполняют разные функции. Сократительные клетки (contractile vSMCs) покрывают поверхность здорового сосуда,
поддерживая его и обеспечивая стабильность. Синтетические (synthetic vSMCs), в том числе мигрирующие, клетки занимаются восстановлением поврежденного сосуда.
(Illustration by Maureen Wanjare)
Работа доктора Герехт и ее коллег может помочь ученым и в понимании того, как стабилизируются кровеносные сосуды, питающие опухоли, что будет полезно при лечении рака.
«Прежде чем нам удастся вырастить совершенно новую сеть кровеносных сосудов в лаборатории, предстоит провести множество исследований, – заключает доктор Герехт, – но наши успехи в контроле над судьбой этих стволовых клеток представляются большим шагом вперед в правильном направлении».
Аннотация к статье
- Источник(и):
- Войдите на сайт для отправки комментариев
 Сайт о нанотехнологиях #1 в России
Сайт о нанотехнологиях #1 в России