Пересаженные нейроны восстанавливают поврежденную нервную цепь и предотвращают ожирение у мышей
Как показывает новое исследование, незрелые нейроны, пересаженные в мозг склонных к ожирению мышей, могут предотвратить развитие ожирения. Ученые, проводившие этот эксперимент, предупреждают, что он ни в коем случае не задуман как шаг на пути к лечению ожирения у людей, но считают, что его результаты являются важным концептуальным доказательствам того, что пересаженные фетальные клетки могут интегрироваться в аномальную нейронную цепь и помочь восстановить ее функцию.
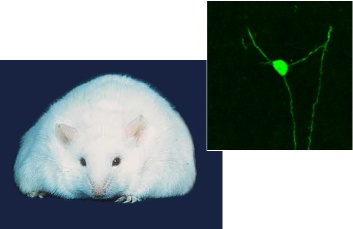 Эксперименты на мышах показывают, что
Эксперименты на мышах показывают, что
пересаженные нейроны могут помочь исправить
генетический дефект, вызывающий ожирение.
(Oak Ridge National Laboratories (мышь);
C. Zhou et al., Science (нейрон))
Дорога к восстановлению нервной системы эмбриональными и другими стволовыми клетками камениста. Вопреки ожиданиям, трансплантации эмбриональных клеток пациентам с болезнью Паркинсона дали неутешительные результаты. Недавно калифорнийская биотехнологическая компания Geron прекратила испытания методов лечения стволовыми клетками спинальных травм, привлекавшие к себе пристальное внимание. Более того, компания сообщила что, по финансовым причинам, вообще отказывается от дальнейшей работы со стволовыми клетками.
Тем не менее, фундаментальные исследования в области неврологии можно признать более обнадеживающими. В последнее десятилетие ученые отказались от вековой догмы, доказав, что в некоторых областях человеческого мозга новые нейроны образуются на протяжении всей жизни. Существуют доказательства, что «новорожденные» нейроны интегрируются в существующие нейронные цепи и помогают поддержанию или улучшению функций мозга. Эти данные позволяют предположить, что и пересаженные клетки в состоянии сделать то же самое.
В новом исследовании, результаты которого опубликованы в журнале Science, невролог из Гарвардского университета (Harvard University) Джеффри Мэклис (Jeffrey Macklis) и его коллеги изучали, могут ли фетальные нейроны, трансплантированные в область мозга мыши, которая обычно не производит собственные новые нервные клетки, восстановить аномальные нейронные цепи. Мыши-реципиенты фетальных нейронов были генетически модифицированы и не имели рецепторов лептина – гормона, регулирующего обмен веществ и массу тела. У нормальных мышей лептин воздействует на нейроны гипоталамуса – области мозга, регулирующей метаболизм и другие жизненно важные функции. Но у мутантных мышей эти нейроны не могут отвечать на лептин, и у животных развиваются диабет и ожирение.
Чтобы проверить, можно ли исправить этот дефект, исследователи пересадили незрелые нейроны, взятые из гипоталамусов плодов мышей с нормальными генами рецептора лептина, в ту же область мозга мышей, склонных к ожирению. Мыши, получившие пересаженные клетки спустя несколько дней после рождения, росли значительно более полными, чем обычные, но не имели патологического ожирения. Грызуны с пересаженными клетками весили в среднем около 40–45 граммов. Для сравнения: обычные мыши весят 25 граммов, в то время как мутантные – от 55 до 60. Кроме того, у мышей с пересаженными нейронами не развивался диабет.
Чтобы исследователь, какова судьба пересаженных нейронов, было использовано несколько методов. В нейроны был встроен ген зеленого флуоресцентного белка, и ученые увидели под микроскопом, что клетки дифференцировались в несколько различных типов нейронов характерных для гипоталамуса и сформировали синаптические связи с другими нейронами. Используя электроды для записи электрической активности нейронов гипоталамуса, исследователи подтвердили, что пересаженные клетки, как и ожидалось, отвечают на лептин и могут взаимодействовать с собственными нейронами мышей-реципиентов.
Доктор Мэклис считает, что извлеченные из этих экспериментов уроки могут помочь ученым, разрабатывающим методы клеточной терапии для таких заболеваний, как боковой амиотрофический склероз, болезнь Паркинсона и травмы спинного мозга. По его мнению, решающее значение здесь будет иметь правильный подбор клеток.
В этом исследовании ученые пересаживали незрелые клетки, которые находились как раз на стадии дифференциации в несколько типов нейронов гипоталамуса. Дополнительные эксперименты показали, что пересаженные мутантным мышам фетальные клетки, взятые чуть позже или из другой части мозга, не предотвращали развития ожирения.
Коллеги гарвардских ученых считают, что эта работа освещает как перспективы, так и проблемы разработки методов клеточной терапии для лечения комплексных мозговых расстройств.
«Работа, безусловно, сделана очень тщательно», – комментирует эксперимент Эван Снайдер (Evan Snyder), занимающийся стволовыми клетками в Медицинском научно-исследовательском институте Сэнфорд-Бернем (Sanford-Burnham Medical Research Institute) в Сан-Диего, Калифорния.
Ее результаты, по его мнению, вносят свой вклад в растущее осознание того, что клеточная терапия должна быть адаптирована к конкретной поврежденной нейронной цепи. На заре исследований в этой области, говорит Снайдер, ученые надеялись, что простая пересадка в мозг стволовых клеток или клеток-предшественников нейронов восстановит нейронные цепи, поскольку сигналы из клеточного окружения скажут новым клеткам, что делать. Однако это оказалось не так.
«Восстановление цепи потребует объединения целого ряда специализированных клеток, и в этом мы не можем полагаться на окружающую среду», – считает Снайдер. «Я по-прежнему настроен оптимистично, но предстоит много тяжелой интеллектуальной работы».
Аннотация к статье
Transplanted Hypothalamic Neurons Restore Leptin Signaling and Ameliorate Obesity in db/db Mice
- Источник(и):
- Войдите на сайт для отправки комментариев
 Сайт о нанотехнологиях #1 в России
Сайт о нанотехнологиях #1 в России